ホーム > 砂糖 > 話題 > 「機能性表示食品制度における機能性関与成分の取扱い等に関する検討会報告書」の概要
最終更新日:2017年6月9日
「機能性表示食品制度における機能性関与成分の取扱い等に関する検討会報告書」
の概要〜機能性表示食品制度における機能性関与成分の取扱い等について〜
2017年6月
国立研究開発法人農業・食品産業技術総合研究機構
食品研究部門 食品機能研究領域長 山本(前田) 万里
食品研究部門 食品機能研究領域長 山本(前田) 万里
1.機能性表示食品制度とは
2015年4月から施行された機能性表示食品制度は、企業などの責任において届け出ることで食品に健康の維持および増進に資する機能性の表示を行うことができる制度である。機能性表示食品は、安全性の確保を第一に考慮し、消費者の誤認を招かない自主的かつ合理的な選択に資するものであることが重要である。世界的にも珍しい届け出制の制度であり、農林水産物も対象とされている。2017年4月21日現在で860を超える食品が届け出・受理されているが、生鮮食品は6品目で、後は加工食品とサプリメントが半分ずつ程度の割合となっている。
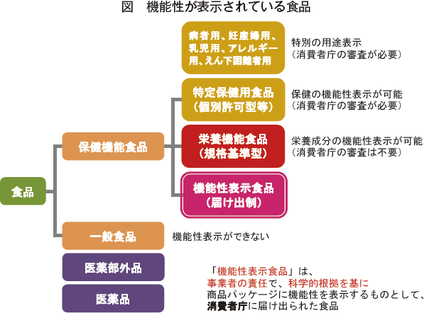
機能性表示制度では、施行時に「栄養成分」および「機能性関与成分が明確でない食品」は対象外であり、その取り扱いが施行後の検討課題とされていた。ここでは、残された課題について検討するため消費者庁で設置された「機能性表示食品制度における機能性関与成分の取扱い等に関する検討会」(2016年1月22日〜 11月25日、全11回開催)で討議された機能性関与成分の取り扱いについて紹介する。
2.現行機能性表示制度での機能性関与成分の考え方
現行法での機能性関与成分の考え方は以下のようなものであった。(1)表示しようとする機能性にかかる作用機序について、in vitro(注1)試験およびin vivo(注2)試験、または臨床試験により考察されているものであり、直接的または間接的な定量確認および定性確認が可能な成分(2)健康増進法(平成14年法律第103号)第16条の2第1項の規定に基づき厚生労働大臣が定める「食事摂取基準」に基準が策定されている栄養素を含め、食品表示基準別表第9の第1欄に掲げる成分−は対象外。なお、一部の栄養素の構成成分については、栄養素との作用の違いなどにより、対象成分となりえる。
(注1)ラテン語で、「試験管内で」という意味。in vivoの対義語で、生体内で営まれている機能や反応を試験管内など生体外に取り出して、各種の実験条件が人為的コントロールされた環境(理想的には、未知の条件がほとんど無い)で起きている反応・状態という意味で使われる。
(注2)ラテン語で、「体内で」という意味。生化学や分子生物学などの分野で、in vitroとは異なり、各種の条件が人為的にコントロールされていない生体内で起きている反応・状態という意味で使われる。
(注2)ラテン語で、「体内で」という意味。生化学や分子生物学などの分野で、in vitroとは異なり、各種の条件が人為的にコントロールされていない生体内で起きている反応・状態という意味で使われる。
3.機能性関与成分の取り扱いの変更点
「機能性表示食品制度における機能性関与成分の取扱い等に関する検討会」では、これから述べる二つの議題が討議され、最終報告書は2016年12月28日に公表された。
まずは、栄養成分の取り扱いについてである。現行法では、「食事摂取基準」に基準が策定されている栄養素を含め、食品表示基準別表第9の第1欄に掲げる成分(タンパク質、脂質、飽和脂肪酸、n-3系脂肪酸、n-6系脂肪酸、コレステロール、炭水化物、糖質、糖類〈単糖類または二糖類であって、糖アルコールでないものに限る〉、食物繊維、亜鉛、カリウム、カルシウム、クロム、セレン、鉄、銅、ナトリウム、マグネシウム、マンガン、モリブデン、ヨウ素、リン、ナイアシン、パントテン酸、ビオチン、ビタミンA、ビタミンB1、ビタミンB2、ビタミンB6、ビタミンB12、ビタミンC、ビタミンD、ビタミンE、ビタミンK、葉酸)は機能性関与成分としては対象外とされている。この対象外となっている栄養成分のうち、糖質、糖類、ビタミン類、ミネラル類の今後の取り扱いについて討議がなされ、最終的に、糖質、糖類を対象とするということで定義付けられた(表)。
機能性関与成分となりえる成分は、主として栄養源(エネルギー源)とされる成分(ブドウ糖、果糖、ガラクトース、ショ糖、乳糖、麦芽糖、でん粉、グリコーゲンなど)を除いた糖質、糖類である。検討会では、二糖類を含む難消化性各種オリゴ糖、糖アルコール、アラビノース、プシコース、パラチノース、ラクトスクロース、アロースなどがそれに当たるのではないかと健康食品産業協議会から意見が出された。表示に当たっては、安全性評価の際、糖質、糖類の製造方法についても考慮し、機能性関与成分としての糖質、糖類のエネルギー量について届け出資料に記載することとされた。生産・製造および品質管理にかかる事項については、現行法と同様に、届け出をしようとする食品に機能性関与成分が表示された量が含まれていることおよび機能性関与成分以外の成分のうち安全性を担保する必要がある成分が製品規格を満たしていることを確認するため、第三者の試験機関において実施した分析試験の成績書を添付することとなっている。また、機能性関与成分および機能性関与成分以外の成分のうち安全性を担保する必要がある成分に関する分析方法を示す資料を添付することとなった。糖質、糖類の分析方法については、妥当性が検証されることが必要であり、査読付き論文や公定法など客観的な評価が行われたものが望ましいとされた。
なお、ビタミン、ミネラルの機能性の表示については、過剰摂取が懸念されることや健康・栄養政策との整合性の観点、栄養機能食品制度との関係から、現時点において本制度の対象としないこととなった(表)。ただし、ビタミン、ミネラルの機能性の表示については、健康・栄養政策との整合性を図りながら、今後、栄養機能食品制度において、別途検討する必要があるという意見が出された。
2番目は、機能性関与成分が明確でない食品の取り扱いについてである。討議の結果、機能性の科学的根拠の一部を説明できる特定の成分が判明しているものの、その特定の成分のみでは機能性の全てを説明することはできない「エキスおよび分泌物」(エキス等)について、機能性関与成分として取り扱うことが可能となった。「エキス」は、単一の植物を基原としたものを対象とし、菌を基原としたエキスは対象外となった。そのため、対象として認められたのは、「植物エキスおよびその分泌物」ということになる。なお、届け出をしようとするエキス等が、科学的根拠が得られたエキス等と同等性が担保されていることが必要である。また、エキス等は、少なくとも一つの指標成分で表示しようとする機能性にかかる作用機序が考察されている必要があり、作用機序は、in vitro試験およびin vivo試験、または臨床試験により考察されていることが必要である。さらに、エキス等の品質保証は、同等性を担保することが基本であり、指標成分の定量確認だけでなく、形態学、分析化学(エキス等の定性的なパターン分析など)、分子生物学などの観点からの基原の保証が必要である。また、エキス等の精製過程の同等性の確認も必要である。エキス等を機能性関与成分として届け出を行うに当たっては、使用している基原の学名および部位を届け出ること、また、エキス等を特徴付ける抽出法がある場合はそれを届け出資料に記載する。機能性関与成分名は、基原について消費者が理解しやすい名称を用いる必要があるとされた。
その他として、これまで非公開とされていた機能性関与成分の定性確認および定量確認の分析法は、原則公開ということになった。
まずは、栄養成分の取り扱いについてである。現行法では、「食事摂取基準」に基準が策定されている栄養素を含め、食品表示基準別表第9の第1欄に掲げる成分(タンパク質、脂質、飽和脂肪酸、n-3系脂肪酸、n-6系脂肪酸、コレステロール、炭水化物、糖質、糖類〈単糖類または二糖類であって、糖アルコールでないものに限る〉、食物繊維、亜鉛、カリウム、カルシウム、クロム、セレン、鉄、銅、ナトリウム、マグネシウム、マンガン、モリブデン、ヨウ素、リン、ナイアシン、パントテン酸、ビオチン、ビタミンA、ビタミンB1、ビタミンB2、ビタミンB6、ビタミンB12、ビタミンC、ビタミンD、ビタミンE、ビタミンK、葉酸)は機能性関与成分としては対象外とされている。この対象外となっている栄養成分のうち、糖質、糖類、ビタミン類、ミネラル類の今後の取り扱いについて討議がなされ、最終的に、糖質、糖類を対象とするということで定義付けられた(表)。
機能性関与成分となりえる成分は、主として栄養源(エネルギー源)とされる成分(ブドウ糖、果糖、ガラクトース、ショ糖、乳糖、麦芽糖、でん粉、グリコーゲンなど)を除いた糖質、糖類である。検討会では、二糖類を含む難消化性各種オリゴ糖、糖アルコール、アラビノース、プシコース、パラチノース、ラクトスクロース、アロースなどがそれに当たるのではないかと健康食品産業協議会から意見が出された。表示に当たっては、安全性評価の際、糖質、糖類の製造方法についても考慮し、機能性関与成分としての糖質、糖類のエネルギー量について届け出資料に記載することとされた。生産・製造および品質管理にかかる事項については、現行法と同様に、届け出をしようとする食品に機能性関与成分が表示された量が含まれていることおよび機能性関与成分以外の成分のうち安全性を担保する必要がある成分が製品規格を満たしていることを確認するため、第三者の試験機関において実施した分析試験の成績書を添付することとなっている。また、機能性関与成分および機能性関与成分以外の成分のうち安全性を担保する必要がある成分に関する分析方法を示す資料を添付することとなった。糖質、糖類の分析方法については、妥当性が検証されることが必要であり、査読付き論文や公定法など客観的な評価が行われたものが望ましいとされた。
なお、ビタミン、ミネラルの機能性の表示については、過剰摂取が懸念されることや健康・栄養政策との整合性の観点、栄養機能食品制度との関係から、現時点において本制度の対象としないこととなった(表)。ただし、ビタミン、ミネラルの機能性の表示については、健康・栄養政策との整合性を図りながら、今後、栄養機能食品制度において、別途検討する必要があるという意見が出された。
2番目は、機能性関与成分が明確でない食品の取り扱いについてである。討議の結果、機能性の科学的根拠の一部を説明できる特定の成分が判明しているものの、その特定の成分のみでは機能性の全てを説明することはできない「エキスおよび分泌物」(エキス等)について、機能性関与成分として取り扱うことが可能となった。「エキス」は、単一の植物を基原としたものを対象とし、菌を基原としたエキスは対象外となった。そのため、対象として認められたのは、「植物エキスおよびその分泌物」ということになる。なお、届け出をしようとするエキス等が、科学的根拠が得られたエキス等と同等性が担保されていることが必要である。また、エキス等は、少なくとも一つの指標成分で表示しようとする機能性にかかる作用機序が考察されている必要があり、作用機序は、in vitro試験およびin vivo試験、または臨床試験により考察されていることが必要である。さらに、エキス等の品質保証は、同等性を担保することが基本であり、指標成分の定量確認だけでなく、形態学、分析化学(エキス等の定性的なパターン分析など)、分子生物学などの観点からの基原の保証が必要である。また、エキス等の精製過程の同等性の確認も必要である。エキス等を機能性関与成分として届け出を行うに当たっては、使用している基原の学名および部位を届け出ること、また、エキス等を特徴付ける抽出法がある場合はそれを届け出資料に記載する。機能性関与成分名は、基原について消費者が理解しやすい名称を用いる必要があるとされた。
その他として、これまで非公開とされていた機能性関与成分の定性確認および定量確認の分析法は、原則公開ということになった。

参考
消費者庁「機能性表示食品制度における機能性関与成分の取扱い等に関する検討会報告書」〈http://www.caa.go.jp/policies/policy/food_labeling/other/pdf/kinousei_kentoukai_161227_0002.pdf〉
消費者庁「機能性表示食品制度における機能性関与成分の取扱い等に関する検討会報告書」〈http://www.caa.go.jp/policies/policy/food_labeling/other/pdf/kinousei_kentoukai_161227_0002.pdf〉
このページに掲載されている情報の発信元
農畜産業振興機構 調査情報部 (担当:企画情報グループ)
Tel:03‐3583‐8713
農畜産業振興機構 調査情報部 (担当:企画情報グループ)
Tel:03‐3583‐8713